Bravo, si vous êtes ici c’est que vous avez déjà avalé une quantité d’informations pharaonique! Ou peut-être cherchez-vous simplement des solutions à ces pathologies? En tout cas vous êtes à la bonne porte. Maintenant que vous êtes au point sur les fonctionnements/dysfonctionnements du myocarde en long et en large, il est temps d’aborder les traitements en réponse à l’angor, l’infarctus et autres cardiopathies coronariennes.
Dans cette partie, nous allons donc nous concentrer davantage sur le mode d’action des Beta-Bloquants cardiosélectifs (de type β-1 ) au sein du système adrénergique, dans le cas des cardiopathies coronariennes.
Qu’est-ce qu’un Beta-Bloquant ?
Il s’agit tout d’abord de molécules utilisées aujourd’hui en cardiologie afin de bloquer l’action d’adrénaline et de noradrénaline (composants du système sympathique). Le β-bloquant est une substance qui a la capacité de se fixer sur les récepteurs β de l’adrénaline mais sans engendrer d’actions stimulantes sur le cœur. Par conséquence, il inhibe la fixation de l’adrénaline sur son récepteur et empêche par cela son action stimulatrice. D’où le terme de bloquant ou « blocker » en Anglais. Récemment il a été montré que le Beta-Bloquant empêche non seulement l’action stimulatrice de l’noradrénaline mais il déclenche aussi un signal de survie des cellules cardiaques que nous appréhenderons par la suite (actuellement, des recherches se font sur ce sujet). Ce double rôle peut donc expliquer son efficacité en tant que protecteur du cœur.
Les effets sur le myocarde sont :
Sur les récepteurs β-1
- Réduction de la fréquence cardiaque
- Diminution de la contractilité myocardique
- Diminution de la vitesse de conduction
- Diminution de l’excitabilité cardiaque
Sur les récepteurs β-2
- Contractions des fibres musculaires lisses du poumon et de l’utérus
En revanche ils sont déconseillés au patient atteint de diabète ou d’asthme car cela peut entraîner des complications. En effet, les récepteur β-1 et β-2 sont présents à de nombreux endroits de l’organisme, bloquer leur action au niveau du coeur peut être bénéfique mais la présence des Beta-bloquants dans le sang aura des conséquences sur tous les organes où ils sont présents.
Un peu d’Histoire sur les Beta-Bloquants
Cette molécule a été inventé par le professeur Sir James Whyte Black ( médecin et pharmacologue écossais) en 1960, qui crée alors le propranolol.

Cette découverte se présente alors comme une révolution dans le traitement de l’angor et lui vaut d’être récompensé du Prix Nobel de physiologie ou médecine en 1988.
Aujourd’hui encore, ces médicaments restent une révolution. Les traitements évoluent et les Beta-bloquants sont même prescrits en cas d’insuffisance cardiaque (pourtant paradoxale) pour maintenir le débit cardiaque. De plus leur propriété dans la survie cellulaire plus récemment découverte, fait des β-bloquants une molécule d’avenir contre les pathologies du cœur.
Cependant certains d’entre-eux, tel que le propranolol sont considérés comme des produits dopants dans certains sports de précision (tir au pistolet, F1 d’après le règlement antidopage de la FIA partie 4.2.2). En effet, par delà ses effets de diminution des influx nerveux sur le coeur, d’augmentation de la contraction des vaisseaux sanguins, de réduction de la consommation en oxygène du cœur et du blocage des fonctions du système nerveux sympathique sur les autres organes, le propranolol inhibe les actions de la noradrénaline, un neurotransmetteur qui facilite la consolidation de la mémoire. Ils peuvent donc réduire ou effacer certaines émotions traumatiques et permettre une plus grande concentration en diminuant le stress.
C’est pourquoi il a couramment été utilisé par les pilotes de F1 qui ont besoin de fournir une effort de longue durée avec une précision hors pair. De même, lors des jeux olympiques d’été de 2008 à Beijing , le Nord-Coréen Kim Jong Su a été contrôlé positif à ce produit lors de la compétition de tir au pistolet, et ses 2 médailles lui ont été retirées. L’effet recherché est le ralentissement du rythme cardiaque et la réduction des tremblements pour favoriser la précision du tir et la concentration.

Par ailleurs, le propranolol a été utilisé par le Ministère de le Défense Américaine à la suite de la guerre du Viêt Nam (1955-1975) qui fut particulièrement traumatique.

Le 8 juin 1972, photo de Nick Ut
De ce fait, le gouvernement américain a participé au financement à hauteur de 5 millions de dollars pour soigner ses soldats (plus de 60 000 soldats américains se sont suicidés après la guerre du Viêt Nam, ce qui dépasse le nombre de soldats tués au combat : 47 539 morts). Les tests sont un succès avec 70 à 80 % de résultats positifs (d’après « En finir avec la peur, comment la science peut agir sur nos souvenirs », reportage diffusé sur Arte, 2011). Le propranolol fait l’objet d’un engouement grandissant car certains chercheurs affirment qu’il permettrait de se remémorer des situations stressantes déjà vécues tout en gommant l’impact émotionnel. Des études ont montré que les individus qui prenaient du propranolol immédiatement après une expérience traumatique montrent moins de symptômes sévères de syndrome de stress post-traumatique que les groupes comparatifs sans traitement. Le propranolol diminue les effets des cauchemars sur l’activité cardiaque en diminuant le rythme sinusal lent pendant les cauchemars.
Comment le médicament se présente-t-il ?
Pour le traitement de la cardiopathie coronarienne le β-bloquant se prend simplement sous la forme d’un cachet.
exemple: Le Propanolol TEVA 40mg comprimé sécable boite de 50.
Traitement:
- en moyenne 4 comprimés/J en 2 prises (160mg)
- traitement institué entre le 5ème et le 21ème jour après l’épisode aigu de l’infarctus
- prix de vente 1.63 euro.
Aujourd’hui le propranolol est moins utilisé et fait place à d’autres β-bloquants tel que l’Acébutolol.
Comment cette molécule agit-elle sur les récepteurs β-1 adrénergiques ?
1) la voie adrénaline fonctionnelle
La plupart des communications entre les cellules se produisent par l’intermédiaire de ligand. Un ligand est une molécule libérée par une cellule qui se fixe à un récepteur membranaire d’une autre cellule. L’noradrénaline (le ligand qui va nous intéresser) est un neurotransmetteur c’est-à-dire qu’il est libéré par des neurones.
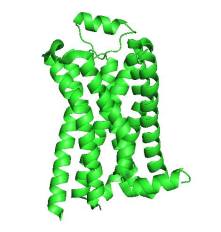
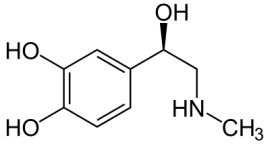
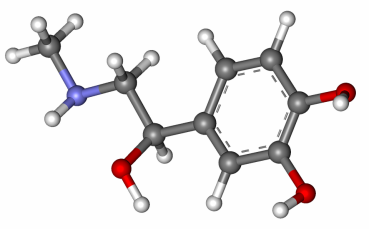
Elle est sécrétée en réponse à un état de stress ou en vue d’une activité physique. La cellule qui la reçoit (ici les cardiomyocytes et les cellules cardionectices) possède à la surface de sa membrane plasmique, un récepteur qui peut fixer le ligand. Cette liaison entraîne une accélération du rythme cardiaque, une augmentation de la vitesse des contractions du cœur et une hausse de la pression artérielle. L’noradrénaline agit donc sur la régulation du rythme cardiaque :
- les récepteurs qui captent les variations de pression artérielle ou de composition du sang ;
- les fibres nerveuses sensitives : dans les nerfs de Hering et de Cyon-Ludwig pour les sinus, et dans la fibre cardiosensible pour l’oreillette droite ;
- le centre nerveux parasympathique, qui est situé dans le bulbe rachidien ; on le nomme centre cardiomodérateur ;
- le centre nerveux sympathique, qui est situé dans la moelle épinière ; il est nommé centre cardio-accélérateur. Entre les deux centres nerveux, des neurones inhibiteurs sont chargés d’affaiblir l’un des deux systèmes quand l’autre est stimulé.
- les fibres nerveuses motrices, regroupées dans le nerf pneumogastrique (ou nerf vague), qui est connecté au nœud sinusal, et dans le nerf cardiaque, connecté au nœud sinusal et aux ventricules.
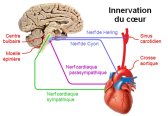

Le mode d’action de l’adrénaline sur le récepteur β-1 adrénergique :
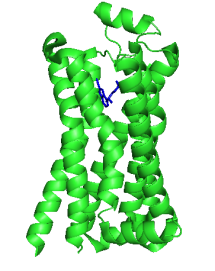
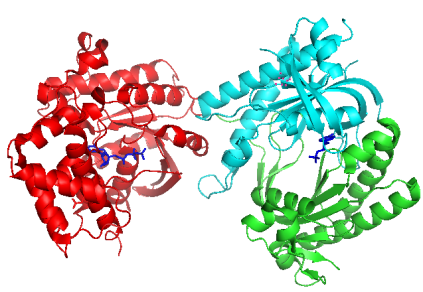
Les récepteurs beta 1 est un récepteur à 7 passages transmembranaires situé sur les cellules cardiaques. Couplés à l’adenylate cyclase par une protéine G, leur stimulation induit la formation d’AMPcyclique à partir d’ATP. C’est donc lui qui va recevoir l’adrénaline en premier lieu.
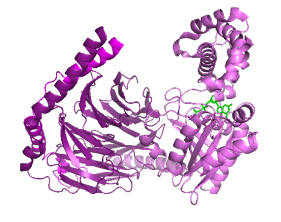
Par ailleurs, la protéine G participe au mécanisme de transduction du signal. C’est à dire qu’elle exécute un transfert d’information intracellulaire par le biais de l’échange de GDP par GTP. Ainsi cette protéine possède un mode de fonctionnement similaire à celui d’un « interrupteur » moléculaire qui déclenche des réactions chimiques à l’image d’un interrupteur lumineux dans un immeuble qui reste activé pendant un certain temps.
Après cette courte explication sur le système de couplage entre ces deux protéines, place à leur interaction :
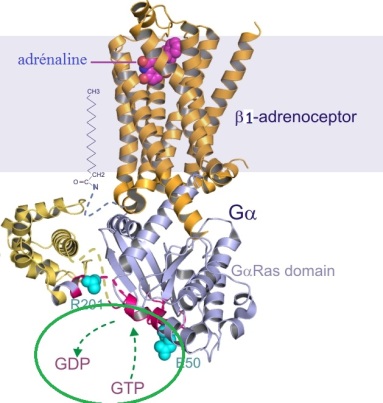
Premièrement, l’adrénaline/noradranéline, présente dans le milieu intercellulaire se fixe sur le récepteur β-1 . Ceci entraîne la liaison et l’activation (excitatrice) de la protéine G au récepteur qui lui est associé. Cela provoque une libération de sa liaison GDP de la sous unité GαRas, et lie une molécule de GTP à la place. Cet échange permet la dissociation de la sous unité GαRas vis à vis du récepteur, de la sous unité β et de la γ, pour venir se lier à l’adénylate cyclase (enzyme transmembranaire). Cette dernière va alors activer une production d’anénosine monophosphate cyclique (AMPc) par hydrolyse de l’ATP présent dans la cellule.
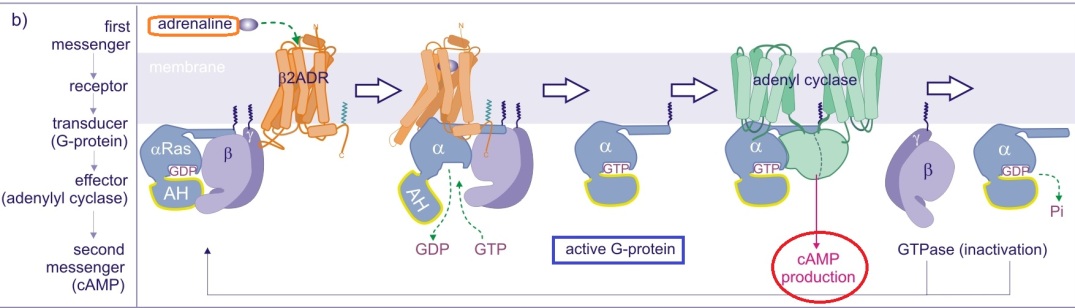
Par ailleurs, le récepteur est de nouveau capable d’activer une nouvelle protéine G. Par son activité enzymatique inhérente, la sous-unité Gα va finir par hydrolyser la GTP en GDP, permettant de se ré-associer avec Gβ et Gγ pour redémarrer un nouveau cycle.
La cascade de réaction entraînée par l’action de l’AMPc:
Ensuite, le second messager, l’AMPc, va activer la protéine kinase A, laquelle va phosphoryler diverses protéines rendant compte de la diversité des effets.

En effet, dans la cellule musculaire cardiaque, la protéine kinase A phosphoryle les canaux à ions Ca2+. Ils s’ouvrent lors de la dépolarisation membranaire induite par le potentiel d’action généré par le nœud sinusal, entraînant un influx calcique important vers l’intérieur de la cellule. Ce calcium (Ca2+) se lie à la troponine C provoquant l’interpénétration des filaments d’actine et de myosine comme vu précédemment. (dans la partie sur les cellules musculaires cardiaques).
La protéine kinase A phosphoryle également les canaux à ions Ca2+ du réticulum sarcoplasmqiue. L’ouverture des canaux calciques du réticulum sarcoplasmique permet d’augmente la quantité de Ca++ disponible pour la contraction. C’est à dire qu’un plus grand nombre d’ion Ca2+ vont se lier avec une troponine pour donc engendrer une contraction plus importante.
De plus, la protéine kinase A accélère le repompage du Ca++ par le réticulum sarcoplasmique en phosphorylant le phospholambdan, protéine qui active l’ATPase calcium-dépendante du réticulum sarcoplasmique responsable du repompage calcique d’où l’accélération de la relaxation de la fibre cardiaque.
La force des contractions cardiaques dépend donc du degré de phosphorylation des canaux calciques et donc de la quantité d’adrénaline de neurotransmetteurs fixés au récepteur.
Elle est ainsi augmentée par la stimulation beta 1 adrénergique.
La fréquence cardiaque, quand à elle, dépend de l’automatisme des cellules du nœud sinusal. Elle est également augmentée par la stimulation des récepteurs β-1 adrénergique qui joue un rôle sur la vitesse de dépolarisation spontanée de ces cellules en activant un courant ionique spécifique.
De même l’augmentation de l’influx calcique augmente la vitesse de dépolarisation initiale des fibres du nœud auriculo-ventriculaire et augmente ainsi sa vitesse de propagation : la vitesse de conduction à travers le nœud auriculo-ventriculaire est ainsi accélérée.
2) Le rôle des β-bloquants dans la voie adrénergique
Enfin, nous y voici, Les β-bloquants.
Les β bloquants viennent se fixer à la place de l’adrénaline/noradrénaline sur de nombreux récepteurs adrénergiques des cardiomyocytes inhibant l’action de la protéine G et donc de toute la chaîne de réactions qui amène à la contraction cardiaque. Ils réduisent donc le travail cardiaque et la consommation myocardique en oxygène. D’où leur intérêt dans l’insuffisance coronarienne, où l’apport en oxygène est insuffisant du fait du rétrécissement du calibre des artères coronaires (sténoses athéromateuses). D’autant que l’effet des beta-bloquants s’accompagne d’une redistribution du débit coronaire vers les couches myocardiques sous endocardiques, les plus sensibles à l’ischémie.
C’est pourquoi on qualifie les β-bloquants « d’antagonistes » à l’adrénaline.
Cependant, il existe d’autres molécules qualifiées de β-« bloquant » mais qui ne sont pas antagonistes de l’adrénaline, c’est à dire qu’elles ont les mêmes effets qu’un « bloquant » puisqu’elles se fixent bien à la place de l’adrénaline sur le récepteur, empêchant la cascade de réaction menant à la contraction. Mais, elles n’inhibent pas toutes réactions de la part de celui-ci. En effet, elles induisent d’autres effets, notamment celui de la signalisation de survie cellulaire.
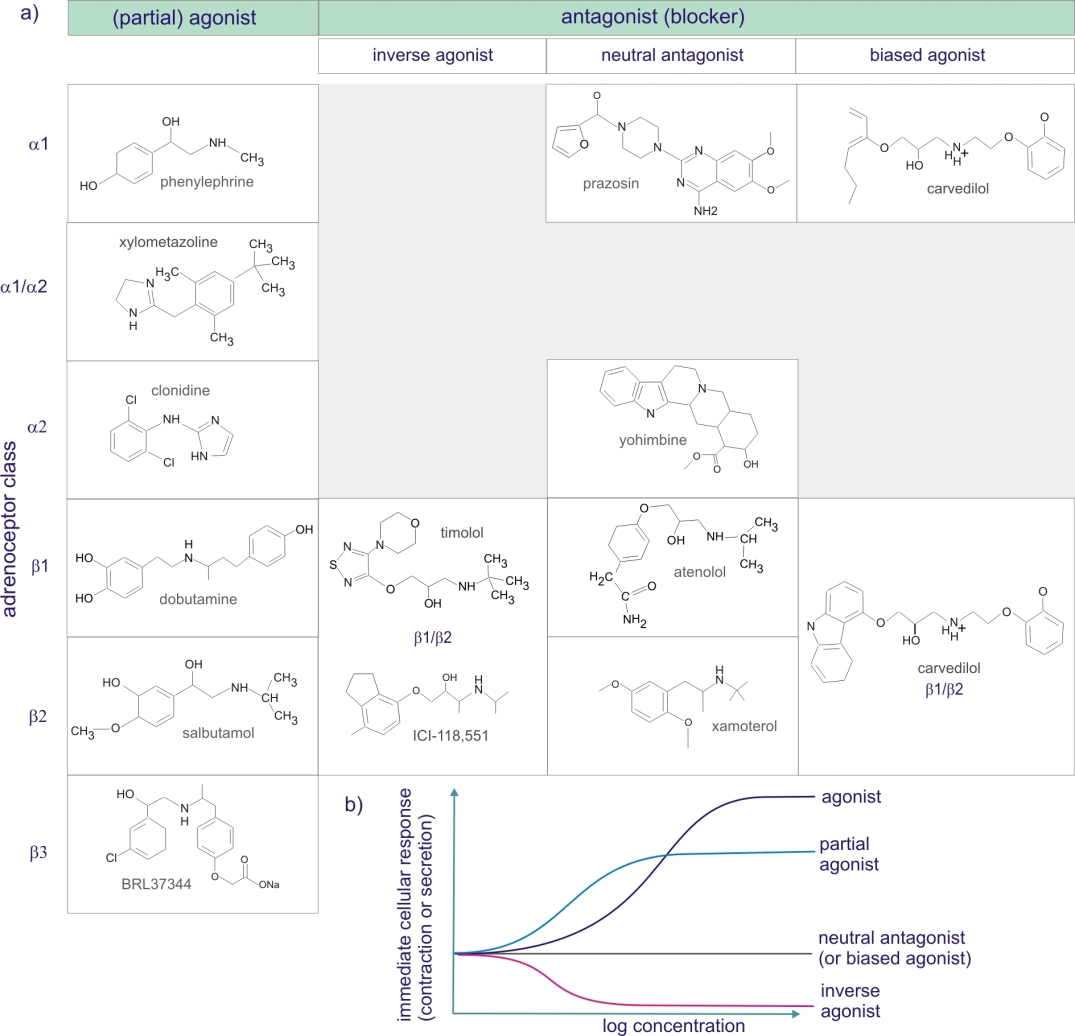
- les antagonistes neutres, qui se fixent sur le site de fixation de l’adrénaline bloquant cette dernière mais n’engendrant aucun signal.
- les agonistes inverses, qui se fixent sur un site de fixation différent entraînant un changement de conformation du récepteur β-1 et qui ne peut plus fixer l’agoniste (adrénaline). Il n’y a pas d’émission de signal (schéma « c »).
- les agonistes partiels, qui jouent à la fois le rôle d’agoniste (le même rôle de l’adrénaline) et d’antagoniste, c’est pourquoi ils ne sont pas qualifiés de « bloquants ». L’agoniste partiel agit comme un antagoniste compétitif, il est en concurrence avec l’agoniste complet (adrénaline) pour l’occupation des récepteurs ; on observe alors une diminution nette de l’activité du récepteur par rapport à celle qu’elle aurait juste avec l’agoniste complet seul.
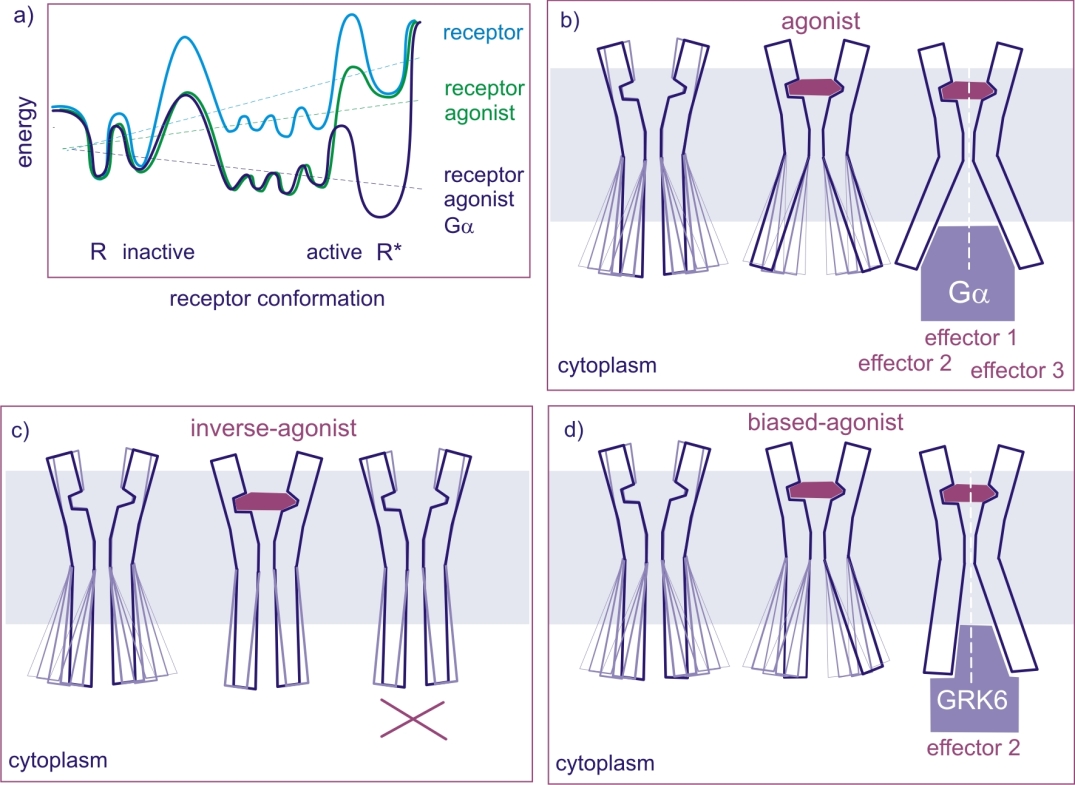
- Les agonistes biaisés, qui vont particulièrement nous intéresser car c’est un agoniste du récepteur β-1 couplé ou pas aux protéines G (GPCR), dont la liaison stabilise une conformation spécifique du récepteur qui n’active alors qu’une des voies de signalisation couplées à ce récepteur. (schéma « d »)
De plus il faut savoir qu’un récepteur possède un niveau d’énergie propre qui oscille naturellement entre plusieurs valeurs (comme le montre le schéma « a » ci-dessous).
Lorsqu’un ligand vient s’y fixer le niveau d’énergie du récepteur change et subit une dépolarisation pour s’abaisser jusqu’à un niveau d’énergie favorable qui correspond aux niveaux d’énergie des « creux » présents sur la courbe. Le récepteur va alors rester un peu plus longtemps dans cette conformation favorable que si il oscillait normalement. Ceci qui va permettre, durant cette courte période, une signalisation particulière de la part du récepteur qui va être dans le cas de la contraction musculaire, une association avec la protéine G (effectrice).
Lorsqu’il s’agit d’un ligand agoniste biaisé, le niveau d’énergie du récepteur va stagner durant un cours instant dans une conformation spécifique qui va favoriser une signalisation particulière selon le ligand fixé.
Le signal en aval (ici la contraction musculaire) d’un récepteur a d’abord été considéré comme spécifique du récepteur avant d’être considéré comme spécifique des ligands puisque selon ceux qui s’y fixent, les récepteurs couplés à une proteine G (RCPG) peuvent adopter non pas deux, mais une multitude d’états conformationnels. Ces états varient en fonction de l’interaction des récepteurs avec un partenaire effecteur (montrer par l’association avec de nombreux ligands) , par exemple les protéines G ou les arrestines-β .
Ces dernières, sont des protéines régulatrices qui se lient au RCPG sous l’action de certains ligands agonistes biaisés spécifiques tels que le carvédilol (considéré comme un β-bloquant) qui va provoquer par préférence le découplage de la protéine G du récepteur et le couplage avec l’arrestine-β , entraînant ainsi la désensibilisation de la réponse. De plus elles jouent un rôle central dans le trafic cellulaire des RCPG.
Les arrestines-β prennent donc la place de la protéine G pour activer une voie de signalisation totalement différente au niveau cardiovasculaire qui serait : une augmentation de l’expression d’une protéine de transport du choléstérol qui régule la synthèse d’aldostérone. Cette hausse des niveaux d’aldostérone circulante contribuerait au remodelage cardiaque et à la progression de l’insuffisance cardiaque. Cette signalisation particulière cardioprotectrice s’active seulement lorsqu’un ligand biaisé tel carvedilol se place dans le récepteur. Cependant ces effets restent encore peu connus et il s’agit ici d’hypothèses mais rassurez-vous, les recherches en cours ne vont pas tarder à aboutir pour nous révéler bien plus encore sur les β-bloquants.



Très bon explication du mode de fonctionnement des b-bloquants, assez simple ce qui est difficilement trouvable sur le net…
J’aimeJ’aime
Merci beaucoup, effectivement c’est un sujet complexe qui aujourd’hui encore n’est pas totalement maîtrisé.
J’aimeJ’aime